Historie HCH
HCH je pojmenována po Georgi Huntingtonovi, americkém lékaři, který chorobu popsal v roce 1872. Popis byl založený na pozorování rodin postižených HCH z vesnice East Hampton na ostrově Long Island ve státě New York (USA), kde Dr. Huntington žil a pracoval. V minulosti byla HCH známá jako Huntingtonova chorea a Tanec svatého Víta.
Příznaky a průběh choroby
HCH je vzácná choroba, která v evropské populaci postihuje 5 až 10 ze 100 000 osob. Podobný výskyt lze pozorovat v zemích, jejichž populace je převážně evropského původu, jako jsou Spojené státy. HCH je méně častá v Asii a Africe, kde se výskyt odhaduje na 1 člověka na 100 000 obyvatel. Pravděpodobnost dědičnosti a rozvoje HCH je u mužů a žen srovnatelná. Pro HCH je charakteristická kombinace poruch motorických (pohybových), kognitivních (například porozumění) a chování (například nálada), ale mohou být uváděny i jiné příznaky. Tyto příznaky HCH se mohou u jednotlivých osob lišit svou vážností, věkem při nástupu choroby a mírou progrese, a to i u členů stejné rodiny. Například jedna osoba může mít velmi zjevné poruchy pohybu, ale pouze lehké psychiatrické příznaky a zhoršení intelektu, zatímco jiná může roky trpět depresemi a úzkostmi, než se ukáží nějaké abnormální pohyby. Nástup HCH se popisuje jako nenápadný, protože je obvykle obtížné určit datum, kdy onemocnění začalo. Faktory ovlivňující věk při nástupu jsou komplexní a jsou předmětem probíhajícího výzkumu. Když vědci pozorovali početné skupiny pacientů s HCH, všimli si souvislosti mezi počtem opakování trinukleotidu a věkem při nástupu příznaků (obrázek dole). To obecně znamená, že čím vyšší je počet opakování sekvence CAG, tím dříve dojde k nástupu příznaků (obrázek dole). Jak ale ukazuje obrázek dole, v případě konkrétního počtu opakování mohou být rozdíly ve věku při vypuknutí choroby až 30 let. To je pravděpodobně dáno vlivem jiných genů, než je HTT (tzv. genetické modifikátory), a faktory prostředí, jako je životní styl a stravování. Z výše uvedeného vyplývá, že je velmi složité přesně odhadnout věk při vypuknutí choroby u kterékoli osoby, která je nositelem expanze HCH. Na základě klasifikace, kterou vytvořil neurolog a specialista na HCH Ira Shoulson z Univerzity v Georgetownu v USA, může být progrese HCH rozdělena do pěti stádií: Pokud začne HCH v mladším věku (před 20. rokem života), samovolné pohyby (chorea) jsou méně nápadným příznakem než zpomalení pohybu (bradykinéze) a ztuhlost (dystonie). Prvotní příznaky juvenilní HCH zahrnují závažné změny chování, problémy s učením a řečí a zhoršení výkonu ve škole. Občas se u HCH vyskytují epileptické záchvaty a častější bývají u mladých pacientů. Obecně je míra progrese juvenilní HCH rychlejší než u formy dospělých pacientů. Pokud HCH začne později v životě, je chorea obvykle výraznějším příznakem než pomalost nebo ztuhlost. V takových případech bývá obtížnější stanovit rodinnou anamnézu, protože rodiče pacienta již možná zemřeli, eventuálně dokonce předtím, než se u nich příznaky choroby projevily. Lidé s HCH neumírají v přímém důsledku choroby, ale spíše kvůli zdravotním problémům, které vznikají následkem oslabeného zdraví. K tomu patří zápal plic (což je příčina úmrtí u třetiny pacientů s HCH), dušení, selhání srdce, úraz hlavy v důsledku pádu a nedostatečná výživa. Výrazně se zvyšuje riziko sebevraždy, která představuje 7 % příčin úmrtí pacientů.Jak častá je HCH?
Jaké jsou příznaky HCH?
Nejčastějšími psychiatrickými příznaky HCH jsou apatie, úzkost, deprese, podrážděnost, výbuchy hněvu, vznětlivost, obsesivně-kompulzivní chování, poruchy spánku a sociální izolovanost. Méně často jsou pak hlášeny mánie a schizofrenie – včetně bludů (falešné představy) a halucinace (osoba vidí, slyší či cítí věci, které ve skutečnosti neexistují). Postižení jednotlivci mohou mít zvláště v počátečních stádiích choroby sebevražedné myšlenky. Většina pacientů s HCH a jejich opatrovníci vnímají poruchy chování jako tíživější než motorické nebo kognitivní poruchy způsobené chorobou.
HCH je charakterizována jako postupné zhoršování intelektu, logického myšlení, úsudku a paměti. Ke kognitivním příznakům patří pomalejší myšlení, obtížnost se koncentrovat, organizovat, plánovat, rozhodovat se a odpovídat na otázky a také problémy s krátkodobou pamětí i řešením problémů a zhoršení schopnosti přijímat a chápat nové informace.
Existuje řada jiných změn, které se mohou vyskytnout v průběhu choroby, včetně nechutenství, ztráty na váze, ztráty sebeúcty, ztráty sexuální touhy a neschopnosti udržet moč a stolici.Kdy se příznaky HCH vyskytnou?
U většiny lidí, kteří jsou nositeli genu HCH, se příznaky rozvinou ve středním věku, čili ve věku od 35 do 55 let. U přibližně 10 % k tomu dojde před 20. rokem života (mají juvenilní formu HCH) a u dalších 10 % se příznaky objeví až po 55. roce života. Obecně HCH postupuje velmi pomalu, takže nemusí být diagnostikována i mnoho let. Průměrná doba trvání nemoci je 15 až 20 let od stanovení diagnózy, ale to se u jednotlivých osob liší a závisí to také na kvalitě poskytované péče pacientovi.
Co určuje věk při nástupu příznaků?
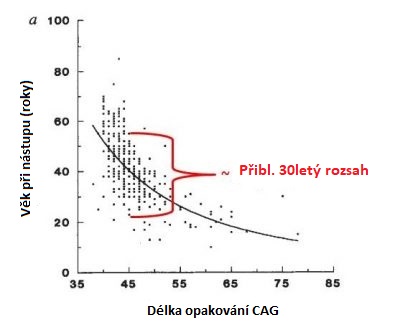
Nature Genetics 4, 398–403 (1993).
Jaká jsou stádia HCH?
Liší se příznaky juvenilní HCH od příznaků v dospělosti?
Jaké jsou příznaky, když HCH začne později v životě?
Příčiny úmrtí
Diagnóza & léčba
HCH se diagnostikuje kombinací klinických hodnocení a genetického testování. Klinická diagnóza je založená na osobní a rodinné anamnéze a také na standardních vyšetřeních, která využívají klinické posuzovací stupnice, aby se zhodnotila četnost a závažnost příznaků HCH. Výsledky klinické diagnózy jsou obvykle potvrzeny genetickým testem expanze HTT (známým jako diagnostické nebo potvrzující genetické testování). Pokud pacient nevykazuje žádné příznaky, ale existuje u něj riziko choroby, asymptomatický genetický test (označovaný jako prediktivní genetický test) určí, zda pacient je, nebo není nositelem genu.Jak se HCH diagnostikuje?
Nástroje klinického hodnocení používané k diagnostikování HCH a měření projevů nejsou ve všech klinikách na světě stejné. Nejčastěji používaným nástrojem je však jednotná škála pro hodnocení Huntingtonovy choroby (Unified Huntington’s Disease Rating Scale, UHDRS), která je rozdělena na dílčí sekce – motorické, kognitivní, funkční a týkající se chování. Kromě toho se v případě Huntingtonovy choroby často používá posouzení problémového chování (Problem Behaviours Assessment, PBA), které pomáhá zhodnotit závažnost a četnost abnormalit v chování (jako je depresivní nálada, apatie a podrážděnost), a různé testy, jako je krátký test kognitivních funkcí (Mini-Mental State Examination, MMSE) a Mattisova škála demence (Mattis Dementia Rating Scale), se zase používají jako doplněk k dílčí sekci UHDRS, která posuzuje kognitivní poruchy.Jaké nástroje klinického hodnocení se ke stanovení diagnózy HCH
používají?
Žít s vědomím, že u vás hrozí HCH, může být velmi stresující. Zřejmě byste chtěli s jistotou vědět, zda nositelem expanze jste, nebo nejste. V takovém případě se velmi doporučuje genetická konzultace a psychologická pomoc, protože vám umožňuje zjistit své možnosti a pohovořit si o svých obavách. Obecně se prediktivní test nedoporučuje osobám mladším 18 let, což je věk, kdy se u člověka předpokládá dostatečná vyzrálost, aby se vypořádal s tím, že je nositelem expanze. Ve výjimečných případech však může být rozumné provést potvrzující genetický test i u dětí – pokud vykazují příznaky juvenilní HCH – nebo u žen mladších 18 let, pokud jsou těhotné. Pokud se rozhodnete test podstoupit, bude vám z žíly na paži odebrán vzorek krve a v laboratoři se z něj získá vaše DNA. V závislosti na místních službách budou výsledky k dispozici do dvou až osmi týdnů. Pracovní skupina pro genetické testování a poradenství při EHDN v roce 2012 aktualizovala směrnice pro postupy prediktivního genetického testování.Jak probíhá prediktivní genetický test?
Genetický test určí počet opakování CAG v genu HTT. Test může zjistit, zda jste nositelem genu HCH, ale nestanoví, kdy choroba vypukne, jak rychle bude postupovat nebo jaké příznaky se u vás rozvinou. Genetický test HCH má téměř 100% přesnost. Výsledky analýzy DNA jsou obvykle překontrolovány za použití druhého vzorku krve. Za účelem potvrzení prvotní diagnózy se navíc může provést analýza krve rodiče postižené osoby (nebo, pokud to není možné, jiného člena rodiny).Co genetický test odhalí?
Ano. Toho lze dosáhnout pomocí moderní diagnostické procedury zvané preimplantační genetická diagnostika (Pre-implantation genetic diagnosis, PGD) – také známé jako vyšetření embrya –, která se používá v kombinaci s oplodněním ve zkumavce (in vitro, IVF) a zahrnuje vyšetření embryí před jejich zavedením do dělohy. Tato technika zajišťuje, že jsou zavedena pouze embrya s normálními kopiemi genu. Pokud je tedy jeden z rodičů nositelem mutace HCH, PGD takovému páru umožňuje počít dítě, které není nositelem mutantního genu HTT, a to bez ohledu na to, zda je nositelem muž, nebo žena. Zákony týkající se ochrany embryí však v některých zemích PGD neumožňují a je také důležité podotknout, že pravděpodobnost otěhotnění po PGD/IVF je nižší než u „přirozeného“ početí. V některých zemích je možné testovat nenarozený plod, který byl počat přirozeně, a zvolit potrat, jakmile je znám jeho genetický stav.Je možné u osoby s genem HCH zajistit, aby HCH nepřenesl na své dítě?
Prenatální diagnóza (před narozením) je k dispozici pouze v případě, že ti, kdo ji požadují, mohou prokázat, že splňují určitá lékařská a právní kritéria specifická pro danou zemi. Pro prenatální diagnózu existují dvě standardní procedury. První je amniocentéza (také nazývaná test plodové vody), kdy je plodová voda obsahující buňky plodu získána pomocí jehly vpíchnuté do břišní stěny matky, a to obvykle ve 14. týdnu těhotenství. Druhou je odběr choriových klků, což zahrnuje odběr vzorku choriových klků placenty. Tuto proceduru lze provést dříve – mezi 10. a 13. týdnem těhotenství. Je však rizikovější pro plod.Mohou se provádět testy na nenarozeném dítěti?
V současnosti neexistuje žádná léčba, která by účinně léčila základní příčiny HCH. Díky teoretickému a klinickému výzkumu jsme však za posledních několik let získali mnohem větší poznatky o HCH a aktuálně také probíhá mnoho studií, které zkoumají patogenezi choroby s cílem identifikovat léky, které posunou nástup nemoci nebo zpomalí její průběh. Zároveň je již k dispozici léčba, která zmírňuje určité příznaky choroby (symptomatická léčba), a tak zlepšuje kvalitu života pacientů. Tato léčba se dělí na farmakologickou (pomocí léků) a nefarmakologickou (bez podávání léků).Lze HCH léčit?
Chorea, bradykinéze, podrážděnost, apatie, deprese, úzkost a poruchy spánku patří k nejtíživějším projevům HCH. Existuje několik způsobů, jak tyto příznaky zmírnit pomocí léků. Řada léků však může mít vedlejší účinky a některé mohou mařit léčebný účinek jiných léků. Určitý lék navíc může mít u různých osob odlišné účinky. Léčbu musí zkušený specialista na HCH přizpůsobit konkrétnímu pacientovi podle jeho příznaků a jeho reakci na dané léky.Jaké jsou farmakologické možnosti při léčbě příznaků HCH?
Nefarmakologická léčba (jako je psychoterapie a kognitivní, pracovní nebo respirační terapie, rehabilitace a logopedie) může zlepšit psychologické a fyzické příznaky HCH. Po takových terapiích například byla hlášena zlepšení v oblasti nálady, motoriky, řeči, rovnováhy, polykání a chůze. Je dobře známé, že cvičení zlepšuje jak tělesné, tak duševní zdraví – celkový stav člověka – a konkrétně se ukázalo, že zmírňuje příznaky deprese. Také se množí důkazy, že může pomoci zpomalit progresi pohybových poruch souvisejících s HCH. Některé fyzioterapeutické programy například prokázaly úspěšné výsledky v oblasti motorických příznaků, chůze a rovnováhy. Fyzioterapeutická pracovní skupina při EHDN například vydala příručku pro fyzioterapeutisty pracující s pacienty s HCH.Jak může pomoci nefarmakologická léčba?
Hodně se diskutuje o přínosech stravy bohaté na vitamíny, koenzymy a další látky, ale ty zatím nebyly klinicky potvrzeny. Vzhledem k tomu, že u některých pacientů s HCH je problémem úbytek na váze, zvláště v pozdějších stádiích nemoci, je důležité v průběhu choroby zajistit zdravé stravování. V pozdějších stádiích může být zapotřebí vysokokalorická strava. Může být užitečné poradit se s odborníkem na výživu.Může příznaky HCH zmírnit speciální dieta?
Dědičnost & a co HCH způsobuje
HCH je způsobena změnou (expanzí) v genu (HTT), který nese kód pro bílkovinu zvanou huntingtin. V důsledku této expanze se gen přemění na upravenou formu bílkoviny, což vede k chybné funkci a úhynu nervových buněk (neuronů) v konkrétních oblastech mozku. Přesné mechanismy choroby jsou mnohostranné a mimořádně složité, což je dáno řadou funkcí bílkoviny huntingtin. Výzkumníci se snaží lépe porozumět základním mechanismům, které chorobu způsobují, aby vyvinuli onemocnění modifikující léčbu.Co způsobuje HCH?
V roce 1993 vědci identifikovali mutaci, která způsobuje HCH. Gen HTT se nachází na 4. chromozomu a nese kód pro bílkovinu zvanou huntingtin. Gen obsahuje sekvenci tří nukleotidů (základní jednotka DNA), cytosin-adenin-guanin (CAG), která se několikrát opakuje. Tato takzvaná repetice/opakování trinukleotidu může mít různou délku. Pokud má člověk v jedné kopii genu HTT 40 a více opakování CAG, nástup nemoci nastane během jeho běžné délky života, také jinak ve středním věku. Vzhledem k tomu, že expanze, která HCH působí, je přítomna ve všech buňkách těla od početí a lze ji přenést na následné generace, považuje se HCH za dědičné onemocnění.Co je základní příčinou HCH?
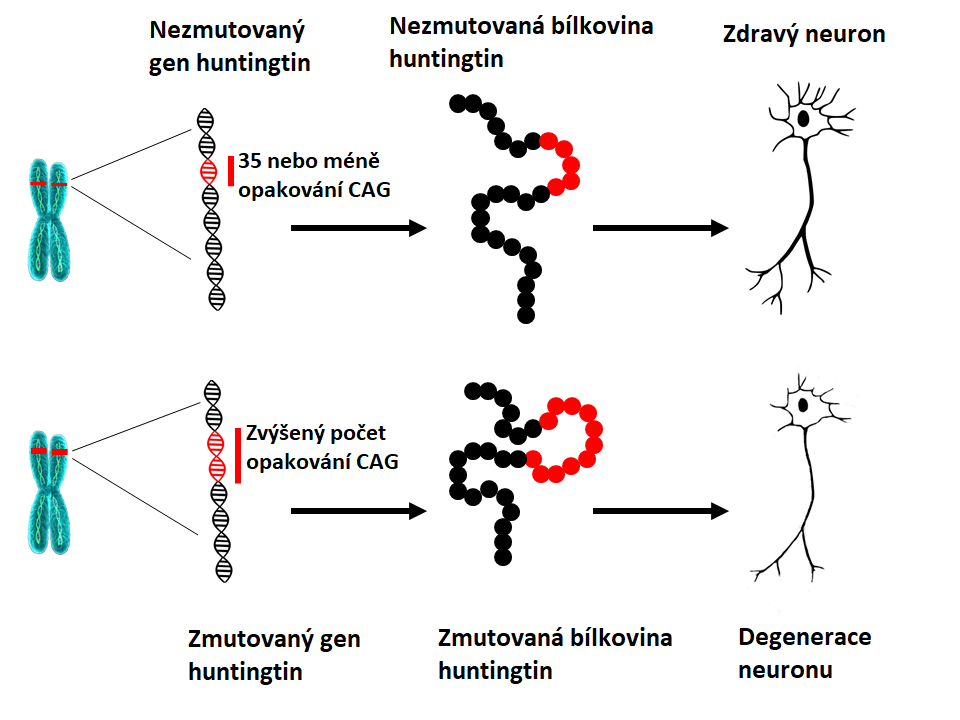
S tím, jak se počet opakování CAG zvyšuje, stávají se určité části DNA méně stabilními. To znamená, že počet opakování v této části se může zvýšit, nebo snížit, když se přenáší na další generaci. Pokud je počet opakování CAG v genu HTT nižší než 27, považuje se daná část za stabilní. Pokud je počet opakování mezi 27 a 35 (takzvaná střední délka repetice), u člověka se HCH nerozvine a tato část se považuje za normální. Počet opakování 27 a více je ale nestabilní a při přenosu na další generaci hrozí jejich navýšení, což znamená, že je u takových dětí riziko rozvoje HCH. U jednotlivců s počtem opakování mezi 36 a 39 může HCH propuknout v pozdním věku, pokud vůbec. Tomuto rozsahu se říká délka repetice se sníženou pronikavostí. Pokud je počet opakování přes 39, nástup nemoci nastane u člověka během jeho běžné délky života, nejčastěji ve středním věku. Ve vzácných případech může být expanze CAG neobvykle dlouhá, což vede k nástupu choroby v dospívání nebo dětství (juvenilní HCH). Pacienti, u kterých se onemocnění projeví před 10. rokem života mají často více než 80 opakování CAG.Co znamená délka opakování CAG u genu HTT?
Délka opakování CAG
Způsobuje chorobu?
Následky pro potomky?
Název
Pod 27
Ne
Žádné
Normální délka opakování
27-35
Ne
27 a více opakování může být nestabilní a může se navýšit při přenosu na potomky
Střední délka opakování
36-39
Možná
Ano, u potomků existuje 50% pravděpodobnost, že zdědí expandovaný gen
Délka opakování se sníženou pronikavostí
40 a více
Ano
Ano, u potomků existuje 50% pravděpodobnost, že zdědí expandovaný gen
Délka opakování s úplnou pronikavostí
Geny se nacházejí v chromozomech uvnitř každé buňky našeho těla. Gen je řetězec DNA, který obsahuje kód pro konkrétní bílkovinu; DNA se přepisuje na mediátorovou RNA (mRNA), která se pak převádí na bílkovinu. Každý člověk obvykle zdědí dvě kopie každého genu – jednu od matky a jednu od otce. V případě HCH je tím důležitým genem HTT, který nese kód pro bílkovinu huntingtin. Pokud dítě zdědí expandovanou verzi genu HTT, pak se i u něj rozvine HCH. Rodič už tuto chorobu může mít nebo u něj vypukne v pozdějším věku.Co je to gen?
Bílkoviny jsou velké molekuly sestavené ze stavebních bloků zvaných aminokyseliny. Přesná sekvence aminokyselin v konkrétní bílkovině je určena sekvencí DNA odpovídajícího genu. Geny proto fungují jako modrotisky – soubor pokynů, které buňkám říkají, jak mají sestavit konkrétní bílkoviny. Gen HTT obsahuje pokyny k tomu, jak sestavit bílkovinu huntingtin. Bílkoviny jsou molekuly, které vykonávají práci uvnitř buněk – provádějí velké množství zásadních procesů, jako jsou enzymové reakce nebo strukturální podpora. Pokud bílkovina pracuje abnormálně nebo v důsledku expanze chybí v genu, který nese její kód, pak to může mít vliv na celou buňku a v konečném důsledku na celý organismus, což někdy vede k onemocnění.Co je to bílkovina?
Bílkovina huntingtin je velmi velkou bílkovinou, která je tvořena nebo „vyjádřena“ v různé míře v každé buňce lidského těla; nejvyšší míry dosahuje v mozku. Huntingtin se jeví jako velmi důležitá bílkovina, protože její absence je pro myší embrya smrtelná. Na jednom konci bílkoviny huntingtin je řetězec opakování konkrétní aminokyseliny zvané glutamin. Tento charakteristický prvek, známý jako opakování polyglutaminu, se normálně skládá z 35 jednotek glutaminu. U lidí, kteří jsou nositelem genu HCH, ale obsahuje minimálně 36 opakování, a je to právě tato expanze polyglutaminu, která vede k chybné funkci bílkoviny.Bílkovina huntingtin
HCH je dominantní dědičnou chorobou. To znamená, že u člověka, který se narodí s jednou kopií mutantního genu HTT, se rozvine HCH, i když je také nositelem normální kopie tohoto genu. Nositel expanze HCH, ať už symptomatický, či nikoliv, může předat buď normální, nebo mutantní kopii genu s 50% pravděpodobností v obou případech (pokud je nositelem expanze pouze na jedné ze dvou kopií genu HTT). Lékařské techniky mohou zajistit, že postižený jednotlivec předá svým dětem pouze normální gen HTT. Na druhé straně u člověka, který nezdědil mutantní gen HTT, se choroba nerozvine a ani jeho dětem toto nebezpečí nehrozí. Expanze HCH nemůže přeskočit jednu generaci potomků. Může se však stát, že nositel expanze zemře předtím, než se příznaky projeví, a jeho děti tak neví, že jim hrozí riziko rozvoje této choroby.Jak se HCH předává?
Určité funkce mozku, jako je schopnost pohybovat se, přemýšlet a mluvit, se v důsledku HCH postupně narušují, protože kritické nervové buňky se poškozují a hynou. Nejvíce zasaženou částí mozku je striatum, což je součást bazálních ganglií, která je umístěna hluboko v centrální oblasti mozku. Striatum se primárně podílí na plánování a řízení pohybů, ale i na mnoha dalších procesech včetně vědomí a emocí. Jak HCH postupuje, ovlivňuje mozkovou kůru, neboli cortex (vnější vrásčitá část mozku), a přispívá ke zhoršení kognitivních funkcí. Obecně způsobuje HCH v průběhu času atrofii celého mozku a zhoršuje obecné funkční schopnosti.Oblasti mozku zasažené HCH
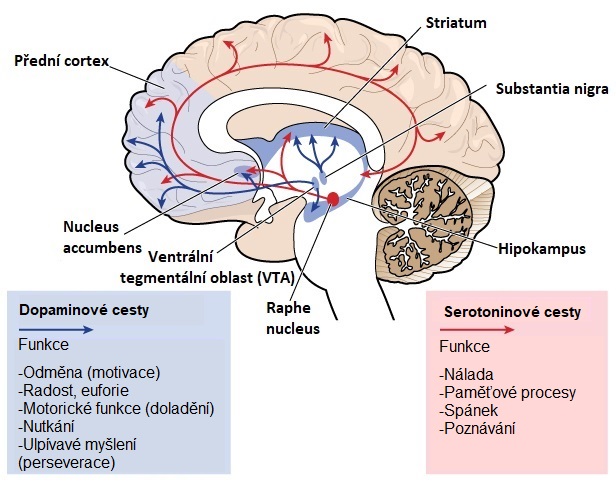
HCH v každodenním životě
Pozitivní test na gen HCH může ovlivnit řadu různých aspektů života člověka: to, zda mít, nebo nemít děti, plánování do budoucnosti, přeuspořádání priorit, sjednání vhodného bydlení nebo sdělení ostatním členům rodiny, že jim také hrozí riziko onemocnění touto chorobou. Zvláště mladí lidé musí zvážit důsledky pozitivního testu na své vzdělávání, praxi a zaměstnání. Jak nemoc postupuje, pomalu zhoršuje schopnost jednotlivce žít nezávisle na druhých. Práce, společenský život a všeobecné každodenní činnosti se stávají problematičtějšími a pacienti jsou čím dál závislejší na pomoci od příbuzných a zdravotních a sociálních pracovníků. Kdykoliv lze kontaktovat místní pacientské organizace a klinická střediska a získat potřebnou podporu.Jaký má HCH vliv na každodenní život?
Účinné strategie pro vypořádání se s HCH musí být přizpůsobeny jednotlivci a odvíjí se od samotné postižené osoby, stádiu choroby a rodinném kontextu. HCH postupuje velice pomalu, takže je obecně čas přizpůsobit se změnám, které přináší. Pečovatelům a blízkým může lepší porozumění poruch chování a kognitivních funkcí spojených s chorobou pomoci vytvořit strategie, díky kterým se změnám lépe přizpůsobí a uchovají si s postiženou osobou dobrý vztah. Užitečné informace se dozvíte od specialistů na HCH a od pacientských organizací.Existují nějaké strategie, které pomáhají se s HCH lépe vyrovnat?
Na této stránce najdete seznam jazykových koordinátorů, kteří vám pomohou. Případně můžete použít zdeuvedený kontaktní formulář.Jak mohou kontaktovat EHDN?
Se specialistou se můžete setkat buď na základě doporučení od praktického lékaře, nebo když kontaktujete místního jazykového koordinátora EHDN, který vám pomůže.Jak si domluvím schůzku se specialistou?
Nezávislé poradenství o HCH lze získat od pacientských organizací ve vaší zemi.Existuje možnost promluvit si se specialistou, aniž bych musel/a navštívit kliniku?
EHDN hraje klíčovou roli v celosvětové klinické studii Enroll-HD. Jedná se o pozorovací studii, která nezahrnuje intervenci. To znamená, že sama o sobě netestuje experimentální léčbu. Účastníci podstupují klinické hodnocení během svým ročních návštěv a mohou být způsobilí pro účast na klinických studiích symptomatické nebo chorobu modifikující léčby, pokud takové studie budou k dispozici. K programu Enroll-HD získáte přístup prostřednictvím mnoha výzkumných center HCH na celém světě. Chcete-li zjistit, zda je takové centrum ve vaší blízkosti, podívejte se prosím zde nebo kontaktujte svého jazykového koordinátora EHDN, který vás bude informovat o výzkumných aktivitách ve vaší oblasti. Místní pacientské organizace vám budou moci poskytnout obecné informace o účasti na výzkumu. Potřebujete-li více informací o výzkumu, podívejte se prosím zde nebo navštivte webovou stránku HDBuzz s novinkami o výzkumu HCH, které píší výzkumníci HCH pro laickou veřejnost a které jsou překládány do mnoha jazyků.Jak se mohu zapojit do výzkumu HCH?
Ano, řadapacientských organizací poskytuje pomoc jednotlivcům a rodinám postiženým HCH. Lze je kontaktovat prostřednictvím vašeho praktického lékaře nebo specialisty na HCH nebo je můžete kontaktovat přímo. Společnost pro pomoc při Huntingtonově chorobě (EHA) vede seznam pacientských organizací, které pro vás mohou být užitečné.Existují organizace, které se specializují na HCH?
Veškeré další otázky vám zodpoví jazykový koordinátor EHDN nebo místní pacientská organizace.

